I/ Synthèse organique
Synthèse d’hétérocycles azotés collaboration avec l’Université Mohamed Ier d’Oujda (Maroc). Cette collaboration consiste en l’élaboration, la synthèse et la détermination de structures de différents hétérocycles à cinq chainons. Les hétérocycles sont des motifs que l’on retrouve dans de nombreuses familles de produits naturels et dans de nombreuses molécules d’intérêt biologique. Nous avons donc synthétisé un grand nombre de di-, tri- et tétrazoles dont l’activité est testée au Laboratoire de Biochimie et Biologie Moléculaire de l’UFR Pharmacie de Reims.
Ce travail s’inscrit dans un projet global qui consiste à développer des monomères entrant dans la synthèse de nouveaux matériaux potentiellement biodégradables ainsi que des matériaux utiles dans la dépollution des eaux usées. La dépollution des eaux usées est un des problèmes environnementaux actuels, trouver des moyens efficaces pour traiter et éliminer des métaux lourds dangereux et toxiques à faibles concentrations est un objectif de ce thème de recherche.
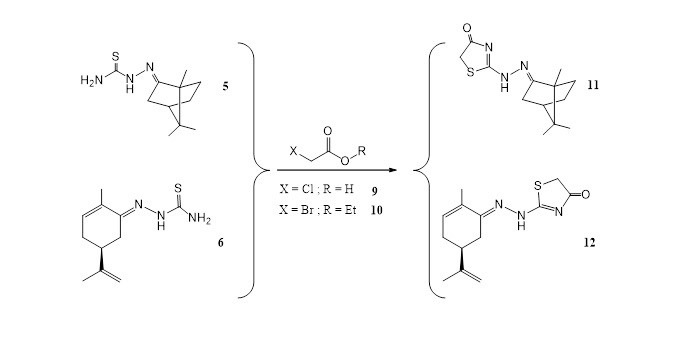
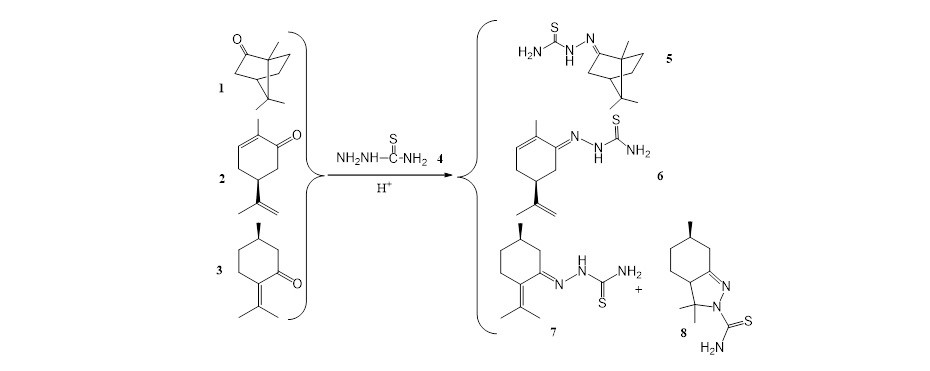
Synthèse de thiazoles et thiadiazoles Une collaboration similaire est conduite avec l’Université Semlalia de Marrakech. Cette collaboration consiste en l’élaboration, la synthèse et la détermination de structures de différents hétérocycles à cinq chainons, utilisant essentiellement la réaction de Huisgen. Nous avons donc synthétisé un grand nombre de thiazoles et thiadiazoles. Des composés de ce type, sont connus pour avoir un large spectre d’activités anti-inflamatoire, antioxydante, antimicrobienne entre autres.